Dernière mise à jour le 08/01/2026
FYREMADEL 0,25 mg/0,5 mL, solution injectable en seringue pré-remplie
Indications thérapeutiques
Classe pharmacothérapeutique : Hormones hypophysaires, de l’hypothalamus et analogues, antagoniste de l’hormone de libération des gonadotrophines, code ATC : H01CC01.
FYREMADEL contient la substance active ganirélix et appartient au groupe des médicaments appelés « antagonistes de l’hormone de libération des gonadotrophines » bloquant les effets de l’hormone naturelle de libération des gonadotrophines (GnRH). La GnRH régule la libération des gonadotrophines (hormone lutéinisante (LH) et hormone folliculo-stimulante (FSH)). Les gonadotrophines jouent un rôle important dans la fertilité humaine et la reproduction. Chez les femmes, la FSH est nécessaire pour la croissance et le développement des follicules dans les ovaires. Les follicules sont de petits sacs ronds qui contiennent les ovocytes. La LH est nécessaire pour libérer les ovocytes matures hors des follicules et des ovaires (c’est-à-dire l’ovulation). FYREMADEL inhibe l'action de la GnRH, résultant en une suppression de la libération de LH en particulier.
Utilisation de FYREMADEL 0,25 mg/0,5 mL, solution injectable en seringue pré-remplie
Chez les femmes ayant recours à des techniques médicales d’assistance à la procréation, telles que la fécondation in vitro (FIV) et d’autres méthodes, l’ovulation peut parfois avoir lieu trop tôt et entraîner une diminution significative des chances de devenir enceinte. FYREMADEL est utilisé pour prévenir le pic prématuré de LH qui est susceptible d’entraîner une libération prématurée des ovocytes.
Dans les études cliniques, le ganirélix a été utilisé en association avec l’hormone folliculo-stimulante recombinante (FSH) ou la corifollitropine alfa, un stimulant folliculaire à longue durée d’action.
Présentations
> 1 seringue(s) préremplie(s) en verre de 0,5 ml munie d'une aiguille d'injection
Code CIP : 275 170-4 ou 34009 275 170 4 4
Déclaration de commercialisation : 25/09/2017
Cette présentation est agréée aux collectivités
- Prix hors honoraire de dispensation : 22,89 €
- Honoraire de dispensation : 1,02 €
- Prix honoraire compris : 23,91 €
- Taux de remboursement :100%
> 5 seringue(s) préremplie(s) en verre de 0,5 ml munie d'une aiguille d'injection
Code CIP : 275 171-0 ou 34009 275 171 0 5
Déclaration de commercialisation : 25/09/2017
Cette présentation est agréée aux collectivités
- Prix hors honoraire de dispensation : 113,12 €
- Honoraire de dispensation : 1,02 €
- Prix honoraire compris : 114,14 €
- Taux de remboursement :100%
Service médical rendu (SMR)
Amélioration du service médical rendu (ASMR)
Ce médicament étant un générique, l'ASMR n'a pas été évalué par la commission de la transparence (CT), il est possible de se référer à la /aux spécialité(s) de référence du groupe générique auquel appartient ce médicament (cliquez ici pour aller à la rubrique des groupes génériques)
Autres informations
- Titulaire de l'autorisation : SUN PHARMACEUTICAL INDUSTRIES EUROPE BV
- Conditions de prescription et de délivrance :
- liste I
- médicament nécessitant une surveillance particulière pendant le traitement
- prescription réservée aux spécialistes et services ENDOCRINOLOGIE
- prescription réservée aux spécialistes et services GYNECOLOGIE
- prescription réservée aux spécialistes et services MALADIES METABOLIQUES
- prescription réservée aux spécialistes et services OBSTETRIQUE
- Statut de l'autorisation : Valide
- Type de procédure : Procédure décentralisée
- Code CIS : 6 146 227 0
ANSM - Mis à jour le : 20/11/2025
FYREMADEL 0,25 mg/0,5 mL, solution injectable en seringue pré-remplie
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Chaque seringue pré-remplie de 0,5 mL contient 0,25 mg de ganirélix sous forme d’acétate).
La substance active, le ganirélix (sous forme d’acétate) (DCI), est un décapeptide synthétique doté d’une haute activité antagoniste de l’hormone naturelle de libération des gonadotrophines (GnRH). Les acides aminés en position 1, 2, 3, 6, 8 et 10 du décapeptide naturel GnRH ont été substitués, donnant le [N-Ac-D-Nal (2)1, D-pClPhe2, D-Pal(3)3, D-hArg(Et2)6, L-hArg(Et2)8, D-Ala10]-GnRH d’un poids moléculaire de 1570,4.
Excipient à effet notoire : sodium. Chaque seringue pré-remplie contient moins de 1 mmol (23 mg) de sodium.
Pour la liste complète des excipients, voir rubrique 6.1.
Solution injectable en seringue pré-remplie.
Solution aqueuse, limpide et incolore avec un pH compris entre 4.5 et 5.5 et une osmolarité comprise entre 250 et 350 mOsm/kg.
4.1. Indications thérapeutiques
Dans les études cliniques, le ganirélix a été utilisé en association avec une hormone folliculo-stimulante humaine recombinante (FSH) ou la corifollitropine alfa, stimulant folliculaire à action prolongée.
4.2. Posologie et mode d'administration
Le ganirélix ne doit être prescrit que par un spécialiste ayant de l’expérience dans le traitement de l’infertilité.
Le ganirélix est administré pour prévenir les pics prématurés de LH chez les femmes en cours d’HOC. L’hyperstimulation ovarienne contrôlée par la FSH ou la corifollitropine alfa peut commencer au 2ème ou au 3ème jour des règles. Le ganirélix (0,25 mg) doit être injecté par voie sous-cutanée une fois par jour, en commençant le 5ème ou le 6ème jour de l’administration de FSH ou le 5ème ou le 6ème jour suivant l’administration de la corifollitropine alfa. Le jour d’initiation du traitement par le ganirélix est déterminé en fonction de la réponse ovarienne, c’est-à-dire du nombre et de la taille des follicules en croissance et/ou du taux d’estradiol circulant.
Le début du traitement par FYREMADEL peut être retardé en l’absence de croissance folliculaire, bien que l’expérience clinique soit basée sur un début de traitement par le ganirélix au 5ème ou au 6ème jour de la stimulation. FYREMADEL et la FSH doivent être administrés approximativement au même moment. Cependant, les préparations ne doivent pas être mélangées et des sites d’injection différents doivent être utilisés.
Les ajustements de dose de FSH doivent être basés sur le nombre et la taille des follicules en voie de maturation, plutôt que sur le taux d’estradiol circulant (voir rubrique 5.1). Le traitement quotidien par FYREMADEL doit être poursuivi jusqu’au jour d’obtention d’un nombre suffisant de follicules de taille adéquate. La maturation finale des follicules peut être induite par l’administration de Gonadotrophine Chorionique Humaine (hCG).
Moment de la dernière injection
En raison de la demi-vie du ganirélix, le délai entre deux injections de FYREMADEL, ainsi que celui entre la dernière injection de FYREMADEL et l’injection d’hCG ne doivent pas dépasser 30 heures, dans le cas contraire, un pic prématuré de LH risque de survenir. En conséquence, lorsque le FYREMADEL est injecté au cours de la matinée, le traitement par FYREMADEL doit être poursuivi pendant toute la période du traitement par la gonadotrophine, y compris le jour de déclenchement de l’ovulation. Lorsque FYREMADEL est injecté au cours de l’après-midi, la dernière injection de FYREMADEL devra être faite dans l’après-midi, la veille du jour de déclenchement de l’ovulation.
Le ganirélix s’est avéré sûr et efficace chez les femmes ayant eu plusieurs cycles de traitement.
Le besoin d’un support de la phase lutéale pendant les cycles sous ganirélix n’a pas été étudié. Dans les études cliniques, le support de la phase lutéale a été fait selon les pratiques habituelles du centre d’étude ou selon le protocole clinique.
Populations particulières
Insuffisance rénale
Les sujets présentant une insuffisance rénale n’étant pas inclus dans les études cliniques, il n’y a pas de données sur l’utilisation du ganirélix chez ces sujets. En conséquence, l’utilisation du ganirélix est contre indiquée chez les patientes présentant une insuffisance rénale modérée ou sévère (voir rubrique 4.3).
Insuffisance hépatique
Les sujets présentant une insuffisance hépatique n’étant pas inclus dans les études cliniques, il n’y a pas de données sur l’utilisation du ganirélix chez ces sujets. En conséquence, l’utilisation du ganirélix est contre indiquée chez les patientes présentant une insuffisance hépatique modérée ou sévère (voir rubrique 4.3).
Population pédiatrique
Il n’y a pas d’utilisation justifiée du ganirélix dans la population pédiatrique.
Mode d’administration
Le ganirélix doit être administré par voie sous-cutanée de préférence dans la cuisse. Pour éviter une lipodystrophie, le point d’injection doit être changé d’une injection à l’autre. La patiente ou son partenaire, peuvent réaliser eux-mêmes les injections de ganirélix, à condition qu’ils aient été convenablement formés et qu’ils aient accès à un avis compétent.
· Hypersensibilité à la substance active ou à l’un des excipients listés à la section 6.1.
· Hypersensibilité à l’hormone de libération des gonadotrophines (GnRH) ou à tout autre analogue de la GnRH.
· Pathologie modérée ou sévère des fonctions rénale ou hépatique.
· Grossesse ou allaitement.
4.4. Mises en garde spéciales et précautions d'emploi
Des précautions particulières doivent être prises chez les femmes présentant des signes et des symptômes de prédisposition allergique. Depuis la commercialisation, des cas de réactions d’hypersensibilité (à la fois généralisées et locales) ont été rapportés avec ganirélix, dès la première dose. Ces événements comprennent anaphylaxie (y compris choc anaphylactique), angio-œdème et urticaire (voir section 4.8). Si une réaction d’hypersensibilité est suspectée, ganirélix doit être arrêté et un traitement approprié administré. En l’absence de données cliniques, un traitement par le ganirélix n’est pas recommandé chez les femmes présentant des risques importants d’allergie.
Allergie au latex
Le capuchon de l’aiguille contient du caoutchouc naturel sec/latex qui entre en contact avec l’aiguille et peut occasionner des réactions allergiques (voir section 6.5).
Syndrome d'hyperstimulation ovarienne (SHSO)
Le syndrome d’hyperstimulation ovarienne (SHSO) peut survenir pendant ou à la suite d'une stimulation ovarienne. Le SHSO doit être considéré comme un risque intrinsèque de la stimulation par une gonadotrophine. Le SHSO doit être traité de façon symptomatique, par exemple par du repos, une perfusion par voie intraveineuse d’une solution d’électrolytes ou de colloïdes et de l’héparine.
Grossesse extra-utérine
Etant donné que les femmes infertiles suivant des techniques d’assistance à la procréation, notamment des fécondations in vitro (FIV), présentent souvent des anomalies tubaires, l’incidence des grossesses extra-utérines peut être augmentée. Il est important de confirmer par une échographie précoce que la grossesse est intra-utérine.
Malformations congénitales
L'incidence des malformations congénitales après des techniques d’Assistance Médicale à la Procréation (AMP) peut être plus élevée qu'après des conceptions spontanées. Ceci semble dû à des différences au niveau des caractéristiques des parents (par exemple âge de la mère, qualité du sperme) et à une augmentation de l'incidence des grossesses multiples. Dans des études cliniques portant sur plus de 1 000 nouveau-nés, il a été démontré que l’incidence des malformations congénitales chez les enfants nés suite à une HOC utilisant le ganirélix était comparable à celle rapportée après HOC utilisant un agoniste de la GnRH.
Femmes pesant moins de 50 kg ou plus de 90 kg
La sécurité et l’efficacité du ganirélix n’ont pas été établies chez les femmes pesant moins de 50 kg ou plus de 90 kg (voir aussi rubriques 5.1 et 5.2).
Ce médicament contient moins de 1 mmol (23 mg) de sodium par injection. Le taux de sodium est inférieur à 1 mmol par injection, c.-à-d. qu’il est essentiellement « sans sodium ».
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Aucune étude d’interaction n’a été réalisée.
La possibilité d’interactions avec des médicaments communément utilisés, y compris les médicaments libérant de l’histamine, ne peut pas être exclue.
4.6. Fertilité, grossesse et allaitement
Grossesse
Il n'existe pas de données pertinentes concernant l'utilisation du ganirélix chez la femme enceinte. Chez les animaux, une exposition au ganirélix au moment de l’implantation a abouti à une résorption de la portée (voir rubrique 5.3). On ignore la pertinence de ces données chez l’homme.
On ignore si le ganirélix est excrété dans le lait maternel.
L’utilisation du ganirélix est contre-indiquée pendant la grossesse et l’allaitement (voir rubrique 4.3).
Fertilité
Le ganirélix est utilisé pour traiter les femmes sous hyperstimulation ovarienne contrôlée dans le cadre des programmes de procréation médicalement assistée. Le ganirélix est utilisé pour prévenir les pics prématurés de LH qui pourraient autrement survenir chez ces femmes pendant la stimulation ovarienne.
Pour la posologie et la méthode d'administration, voir la rubrique 4.2.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Les effets sur l’aptitude à conduire des véhicules et à utiliser des machines n’ont pas été étudiés.
Résumé du profil de sécurité
Le tableau ci-dessous présente tous les effets indésirables rapportés dans les études cliniques chez les femmes traitées par le ganirélix en association avec la FSHrec pour la stimulation ovarienne. Des effets indésirables similaires sont attendus avec le ganirélix utilisé en association avec la corifollitropine alfa pour la stimulation ovarienne.
Tableau des effets indésirables
Les effets indésirables sont classés conformément au système classe- organe MedDRA et à la fréquence : très fréquent (≥ 1/10) ; fréquent (≥ 1/100, < 1/10) ; peu fréquent (≥ 1/1000, < 1/100). La fréquence des réactions d’hypersensibilité (très rare, <1/10 000) est issue de l’expérience post-marketing.
|
Classe de systèmes d’organes |
Fréquence |
Effet indésirable |
|
Affections du système immunitaire |
Très rare |
Réactions d’hypersensibilité (incluant éruption cutanée, gonflement du visage, dyspnée, anaphylaxie (y compris choc anaphylactique), angio-œdème et urticaire)1 Aggravation d’un eczéma pré-existant2 |
|
Affections du système nerveux |
Peu fréquent |
Céphalées |
|
Affections gastro-intestinales |
Peu fréquent |
Nausées |
|
Troubles généraux et anomalies au site d’administration |
Très fréquent |
Réaction cutanée locale au site d’injection (principalement rougeur, avec ou sans gonflement)3 |
|
Peu fréquent |
Malaises |
1Des cas ont été signalés, dès la première dose, chez des patients recevant le ganirélix.
2 Rapporté chez un sujet après la première dose du ganirélix.
3 Dans les études cliniques, une heure après l'injection, 12 % des patientes traitées par le ganirélix et 25 % des patientes traitées par un agoniste de la GnRH par voie sous cutanée ont rapporté une réaction cutanée locale modérée ou sévère survenue au moins une fois par cycle de traitement. Les réactions locales disparaissent en général dans les 4 heures suivant l’administration.
Description d’une sélection d’effets indésirables
Les autres effets indésirables rapportés sont liés à l’hyperstimulation ovarienne contrôlée dans le cadre des techniques d’AMP, notamment douleur pelvienne, distension abdominale, SHSO (voir également rubrique 4.4), grossesse ectopique et avortement spontané.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr.
Un surdosage peut aboutir à une durée d’action prolongée.
Aucune donnée sur la toxicité aiguë du ganirélix chez l’homme n’est disponible. Les études cliniques avec administration sous-cutanée de ganirélix à des doses uniques allant jusqu’à 12 mg n’ont pas révélé d'effet indésirable systémique. Il a été seulement observé au cours des études de toxicité aiguë chez les rats et les singes, des symptômes de toxicité non spécifique, tels que hypotension et bradycardie, après administration intraveineuse de ganirélix avec, respectivement, plus de 1 et 3 mg/kg.
En cas de surdosage, le traitement par le ganirélix doit être (temporairement) arrêté.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Mécanisme d’action
Le ganirélix est un antagoniste de la GnRH, qui module l’axe hypothalamo-hypophyso-gonadique en se liant de façon compétitive aux récepteurs de la GnRH dans l’hypophyse. De ce fait, une suppression rapide, profonde et réversible des gonadotrophines endogènes survient, sans la stimulation initiale que l’on constate avec les agonistes de la GnRH. A la suite de l’administration de multiples doses de 0,25 mg de ganirélix à des femmes volontaires, les concentrations sériques en LH diminuaient au maximum de 74 %, 4 heures après l’injection et celles en FSH et E2 respectivement de 32 % et 25 %, 16 heures après l’injection. Les taux sériques hormonaux revenaient aux valeurs de prétraitement dans les 2 jours suivant la dernière injection.
Effets pharmacodynamiques
Chez les patientes en cours de stimulation ovarienne contrôlée, la durée médiane du traitement avec le ganirélix était de 5 jours. Pendant le traitement par le ganirélix, l’incidence moyenne des élévations de LH (> 10 UI/L) avec une élévation concomitante de la progestérone (> 1 ng/mL) a été de 0,3 - 1,2 % comparée à 0,8 % pendant le traitement par agoniste de la GnRH. On a observé une tendance à l’augmentation de l’incidence des élévations de LH et de la progestérone chez les femmes présentant un poids corporel élevé (> 80 kg), mais aucun effet sur les résultats cliniques n’a été observé. Cependant, étant donné le faible nombre de patientes traitées à ce jour, un effet ne peut pas être exclu. En cas de réponse ovarienne importante, résultant soit d’une forte exposition aux gonadotrophines au début de la phase folliculaire soit d’une haute réactivité ovarienne, des pics prématurés de LH peuvent survenir plus tôt que le 6ème jour de stimulation. L'initiation du traitement par le ganirélix au 5ème jour de la stimulation peut empêcher ces pics prématurés de LH sans compromettre les résultats cliniques.
Efficacité et sécurité cliniques
Dans les études contrôlées avec le ganirélix associé à la FSH, utilisant un protocole long avec un agoniste de la GnRH comme référence, le traitement par le ganirélix a permis une croissance folliculaire plus rapide pendant les premiers jours de stimulation, mais la cohorte de follicules en voie de maturation finale était légèrement plus réduite et a sécrété en moyenne des taux moindres d’estradiol. Ce profil différent de la croissance folliculaire nécessite que les ajustements des doses de FSH soient basés sur le nombre et la taille des follicules en voie de maturation, plutôt que sur le taux d’estradiol circulant. Des études cliniques comparatives similaires avec la corifollitropine alfa utilisant soit un antagoniste de la GnRH soit un protocole agoniste long n’ont pas été réalisées.
5.2. Propriétés pharmacocinétiques
L’analyse pharmacocinétique indique une relation inverse entre le poids corporel et les concentrations sériques de ganirélix.
Absorption
Après une administration unique sous-cutanée de 0,25 mg, les taux sériques de ganirélix augmentent rapidement et atteignent leurs niveaux maximaux (Cmax) approximativement de 15 ng/mL en 1 à 2 heures (Tmax). La biodisponibilité du ganirélix après administration sous-cutanée est d’environ 91 %.
Biotransformation
Le composant principal circulant dans le plasma est le ganirélix. Le ganirélix est aussi le composant principal trouvé dans l’urine. Les fèces ne contiennent que des métabolites. Les métabolites sont des petits fragments peptidiques formés par hydrolyse enzymatique du ganirélix survenant en des sites limités. Le profil métabolique du ganirélix chez l’homme est semblable à celui trouvé chez l’animal.
Elimination
La demi-vie d’élimination (t½) est d’environ 13 heures et la clairance est d’environ 2,4 L/h. L’excrétion se fait par les fèces (environ 75 %) et l’urine (environ 22 %).
5.3. Données de sécurité préclinique
Des études de reproduction réalisées avec le ganirélix chez le rat à des doses allant de 0,1 à 10 microgrammes/kg/jour par voie sous-cutanée et chez le lapin à des doses allant de 0,1 à 50 microgrammes/kg/jour par voie sous-cutanée ont montré une augmentation du taux de résorption des portées dans les groupes de dose les plus élevées. Aucun effet tératogène n’a été observé.
2 ans.
6.4. Précautions particulières de conservation
Ce médicament ne nécessite pas de précautions particulières de conservation.
6.5. Nature et contenu de l'emballage extérieur
Seringue pré-remplie en verre incolore (type I), contenant 0,5 mL de solution injectable stérile, prête à l’emploi, fermée par un bouchon-piston en caoutchouc gris fixé sur la tige d’un piston en polypropylène. Chaque seringue pré-remplie est munie d’une aiguille d’injection (27 G) protégée par un protège-aiguille en élastomère gris et une coque rigide en polypropylène. Chaque seringue pré-remplie est munie d’une aiguille protégée par un capuchon en caoutchouc naturel sec/latex qui entre en contact avec l’aiguille.
Boîtes de 1 ou 5 seringues pré-remplies.
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation
Examinez la seringue avant utilisation. N’utilisez la seringue que si la solution est limpide, ne contient pas de particules et que si son conditionnement n’a pas été endommagé.
Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
SUN PHARMACEUTICAL INDUSTRIES EUROPE B.V.
POLARISAVENUE 87
2132 JH HOOFDDORP
PAYS-BAS
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 275 170 4 4 : 0,5 mL en seringue pré-remplie (verre) + aiguille d'injection, boîte de 1.
· 34009 275 171 0 5 : 0,5 mL en seringue pré-remplie (verre) + aiguille d'injection, boîte de 5.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste I
Médicament à prescription réservée aux spécialistes en endocrinologie ou en gynécologie ou en maladies métaboliques ou en obstétrique.
Médicament nécessitant une surveillance particulière pendant le traitement.
ANSM - Mis à jour le : 20/11/2025
FYREMADEL 0,25 mg/0,5 mL, solution injectable en seringue pré-remplie
Ganirélix
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin, votre pharmacien ou votre infirmier/ère.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
2. Quelles sont les informations à connaître avant d'utiliser FYREMADEL 0,25 mg/0,5 mL, solution injectable en seringue pré-remplie ?
3. Comment utiliser FYREMADEL 0,25 mg/0,5 mL, solution injectable en seringue pré-remplie ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver FYREMADEL 0,25 mg/0,5 mL, solution injectable en seringue pré-remplie ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE FYREMADEL 0,25 mg/0,5 mL, solution injectable en seringue pré-remplie ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique : Hormones hypophysaires, de l’hypothalamus et analogues, antagoniste de l’hormone de libération des gonadotrophines, code ATC : H01CC01.
FYREMADEL contient la substance active ganirélix et appartient au groupe des médicaments appelés « antagonistes de l’hormone de libération des gonadotrophines » bloquant les effets de l’hormone naturelle de libération des gonadotrophines (GnRH). La GnRH régule la libération des gonadotrophines (hormone lutéinisante (LH) et hormone folliculo-stimulante (FSH)). Les gonadotrophines jouent un rôle important dans la fertilité humaine et la reproduction. Chez les femmes, la FSH est nécessaire pour la croissance et le développement des follicules dans les ovaires. Les follicules sont de petits sacs ronds qui contiennent les ovocytes. La LH est nécessaire pour libérer les ovocytes matures hors des follicules et des ovaires (c’est-à-dire l’ovulation). FYREMADEL inhibe l'action de la GnRH, résultant en une suppression de la libération de LH en particulier.
Utilisation de FYREMADEL 0,25 mg/0,5 mL, solution injectable en seringue pré-remplie
Chez les femmes ayant recours à des techniques médicales d’assistance à la procréation, telles que la fécondation in vitro (FIV) et d’autres méthodes, l’ovulation peut parfois avoir lieu trop tôt et entraîner une diminution significative des chances de devenir enceinte. FYREMADEL est utilisé pour prévenir le pic prématuré de LH qui est susceptible d’entraîner une libération prématurée des ovocytes.
Dans les études cliniques, le ganirélix a été utilisé en association avec l’hormone folliculo-stimulante recombinante (FSH) ou la corifollitropine alfa, un stimulant folliculaire à longue durée d’action.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER FYREMADEL 0,25 mg/0,5 mL, solution injectable en seringue pré-remplie ?
N’utilisez jamais FYREMADEL 0,25 mg/0,5 mL, solution injectable en seringue pré-remplie :
· si vous êtes allergique au ganirélix ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6 ;
· si vous êtes allergique (hypersensible) à l’hormone de libération des gonadotrophines (GnRH) ;
· ou à un analogue de la GnRH ;
· si vous présentez une maladie modérée ou sévère, du rein ou du foie ;
· si vous êtes enceinte ou si vous allaitez.
Avertissements et précautions
Adressez-vous à votre médecin, pharmacien ou infirmier/ère avant d’utiliser FYREMADEL 0,25 mg/0,5 mL, solution injectable en seringue pré-remplie :
· si vous avez des prédispositions allergiques, veuillez-en parler à votre médecin. Votre médecin décidera en fonction de leur sévérité si une surveillance supplémentaire est nécessaire pendant le traitement. Des cas de réactions allergiques ont été rapportés, dès la première dose ;
· des réactions allergiques, à la fois généralisées et locales (urticaire), gonflement du visage, des lèvres, de la langue et/ou de la gorge pouvant provoquer des difficultés à respirer et/ou à avaler (angio-œdème et/ou anaphylaxie) ont été rapportées (voir aussi rubrique 4.). Si vous développez une réaction allergique, arrêtez de prendre Fyremadel et consultez immédiatement un médecin.
· allergie au latex, le capuchon de l’aiguille contient du caoutchouc naturel sec/latex qui entre en contact avec l’aiguille et peut occasionner des réactions allergiques.
· pendant ou à la suite d’une stimulation hormonale des ovaires, un syndrome d’hyperstimulation ovarienne peut se développer. Ce syndrome est lié au traitement de stimulation par les gonadotrophines. Veuillez-vous rapporter à la notice du médicament contenant de la gonadotrophine qui vous a été prescrit ;
· l’incidence des malformations congénitales après des techniques d’assistance médicale à la procréation peut être légèrement plus élevée qu’après des conceptions spontanées. Cette incidence légèrement plus élevée semble être liée aux caractéristiques des patientes suivant un traitement pour la fertilité (ex : âge de la femme, caractéristiques du sperme) et à une augmentation de l’incidence des grossesses multiples après des techniques d’assistance médicale à la procréation. L’incidence des malformations congénitales après des techniques d’assistance médicale à la procréation utilisant le ganirélix est comparable à celle rapportée après utilisation d’autres analogues de la GnRH au cours des techniques d’assistance médicale à la procréation ;
· il y a une légère augmentation du risque de grossesse hors de l’utérus (grossesse ectopique) chez les femmes présentant une anomalie des trompes de Fallope ;
· l’efficacité et la sécurité du ganirélix n’ont été établies que chez les femmes pesant entre 50 kg et 90 kg. Pour plus d’informations, adressez-vous à votre médecin.
Enfants et adolescents
Il n’y a pas d’utilisation justifiée de FYREMADEL chez les enfants ou les adolescents.
Autres médicaments et FYREMADEL 0,25 mg/0,5 mL, solution injectable en seringue pré-remplie ?
Informez votre médecin ou pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament.
FYREMADEL 0,25 mg/0,5 mL, solution injectable en seringue pré-remplie avec des aliments, boissons et de l’alcool
Sans objet.
Grossesse, allaitement et fertilité
FYREMADEL est indiqué pour une stimulation ovarienne contrôlée dans le cadre d’une assistance médicale à la procréation (AMP). N’utilisez pas FYREMADEL pendant la grossesse et l’allaitement.
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou pharmacien avant de prendre ce médicament.
Conduite de véhicules et utilisation de machines
Les effets sur l’aptitude à conduire des véhicules et à utiliser des machines n’ont pas été étudiés.
FYREMADEL 0,25 mg/0,5 mL, solution injectable en seringue pré-remplie contient du sodium
Ce médicament contient moins de 1 mmol (23 mg) de sodium par injection, c.-à-d. qu’il est essentiellement « sans sodium ».
3. COMMENT UTILISER FYREMADEL 0,25 mg/0,5 mL, solution injectable en seringue pré-remplie ?
FYREMADEL est utilisé dans le cadre de traitements d’assistance médicale à la procréation (AMP) y compris les fécondations in vitro (FIV).
Étape 1
La stimulation ovarienne par l’Hormone Folliculo-Stimulante (FSH) ou la corifollitropine peut commencer au 2ème ou au 3ème jour de vos règles.
Étape 2
FYREMADEL (0,25 mg) doit être injecté juste sous la peau une fois par jour, en commençant le 5ème ou le 6ème jour de la stimulation. En fonction de votre réponse ovarienne, votre médecin peut décider de commencer le traitement un autre jour.
FYREMADEL et la FSH doivent être administrés approximativement au même moment. Toutefois, les préparations ne doivent pas être mélangées et des sites d’injection différents doivent être utilisés.
Étape 3
Le traitement quotidien par FYREMADEL doit être poursuivi jusqu'au jour où un nombre suffisant de follicules de taille adéquate sont présents. La maturation finale des ovocytes contenus dans les follicules peut être induite par administration de gonadotrophine chorionique humaine (hCG). Le délai entre deux injections de FYREMADEL, ainsi que celui entre la dernière injection de FYREMADEL et l'injection d'hCG ne doit pas dépasser 30 heures car, dans le cas contraire, une ovulation prématurée (libération des ovocytes) peut survenir. Par conséquent, quand FYREMADEL est injecté au cours de la matinée, le traitement avec FYREMADEL devra être poursuivi durant toute la période de traitement par la gonadotrophine, y compris le jour de déclenchement de l’ovulation. Quand FYREMADEL est injecté au cours de l’après-midi, la dernière injection de FYREMADEL devra être faite dans l’après-midi, la veille du jour de déclenchement de l’ovulation.
Mode d'emploi
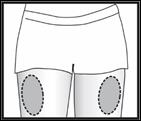
Zone d’injection
FYREMADEL est fourni en seringues pré-remplies et doit être injecté lentement, juste sous la peau, de préférence dans la cuisse. Examinez la solution avant utilisation. Ne pas l’utiliser si elle contient des particules ou si elle n’est pas limpide. Si vous pratiquez vous-même les injections ou si elles sont faites par votre partenaire, respectez strictement le mode d'emploi ci-dessous. Ne pas mélanger FYREMADEL avec d’autres médicaments.
|
|
|
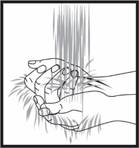
Préparation de la zone d'injection
Lavez-vous minutieusement les mains à l'eau et au savon. Nettoyez la zone d'injection avec un désinfectant (par exemple: alcool) afin d'éliminer toutes les bactéries cutanées. Désinfectez sur une zone d’environ 5 cm (2 pouces) autour du point d'injection et laissez sécher le désinfectant pendant au moins une minute avant de pratiquer l’injection.
|
|
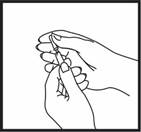
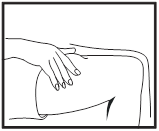
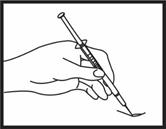
Introduction de l'aiguille
Retirez le capuchon de l'aiguille. Pincez une large zone de peau entre le pouce et l'index. Introduisez l'aiguille à la base de la peau pincée, selon un angle de 45°C par rapport à la surface de la peau.
Changez de point d'injection à chaque injection.
|
|
|
|
Vérification de la position correcte de l'aiguille
Tirez doucement le piston pour vérifier que l’aiguille soit correctement placée. Toute présence de sang dans la seringue signifie que l’extrémité de l'aiguille a pénétré un vaisseau sanguin. Dans ce cas, n’injectez pas FYREMADEL, mais retirez la seringue, couvrez le site d'injection d'un coton imbibé de désinfectant et exercez une pression; le saignement doit cesser en une ou deux minutes. N’utilisez plus cette seringue, et jetez-la soigneusement. Recommencez avec une nouvelle seringue.
Injection de la solution
Une fois l'aiguille correctement positionnée, poussez le piston lentement et régulièrement, la solution sera ainsi correctement injectée et les tissus cutanés ne seront pas abimés.
Retrait de la seringue
Retirez rapidement la seringue et exercez une pression sur le point d’injection avec un coton imbibé de désinfectant. N’utilisez la seringue pré-remplie qu’une seule fois.
|
|
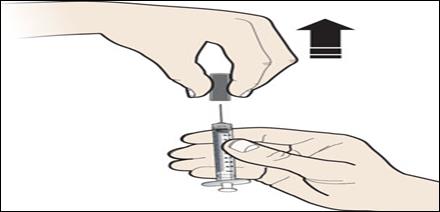
Précautions d'utilisation pour les seringues préremplies
Ce produit est contenu dans une seringue munie d'une aiguille fine. Tenez la seringue préremplie par le milieu du cylindre en verre en la retirant de son contenant pour éviter de courber ou d’endommager l’aiguille.
|
Ne pas utiliser la seringue préremplie en cas d’anomalie ou si l’aiguille semble courbée : Inspectez soigneusement la seringue et l’aiguille avant utilisation. Si l’aiguille présente une courbure ou des signes de détérioration, n’utilisez pas la seringue. Contactez votre professionnel de santé ou votre pharmacien. |
|
|
Ne pas retirer le capuchon de l’aiguille puis le remettre en place : Une fois le capuchon de l’aiguille retiré, ne tentez pas de le remettre en place. Cette action pourrait endommager ou courber l’aiguille, ce qui pourrait entraîner une administration incorrecte ou un risque de blessure. |
|
|
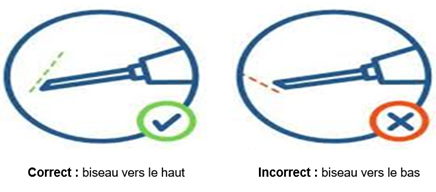
Veiller à orienter le biseau de l’aiguille vers le haut (et non vers le bas) : Lors de l’administration de l’injection, assurez-vous que le biseau de l’aiguille est orienté vers le haut pour éviter la douleur et la flexion de l’aiguille. Cette position permet une insertion facilitée et une injection sécurisée. |
|
Si vous avez utilisé plus de FYREMADEL 0,25 mg/0,5 mL, solution injectable en seringue pré-remplie que vous n’auriez dû :
Consultez immédiatement votre médecin.
Si vous oubliez d’utiliser FYREMADEL 0,25 mg/0,5 mL, solution injectable en seringue pré-remplie :
N’injectez pas de dose double pour compenser la dose que vous avez oubliée d’injecter.
Si le retard est supérieur à 6 heures (de sorte que l'intervalle entre deux injections dépasse les 30 heures), injectez la dose aussitôt que possible, et contactez votre médecin pour qu’il vous conseille.
Si vous arrêtez d’utiliser FYREMADEL 0,25 mg/0,5 mL, solution injectable en seringue pré-remplie :
N’arrêtez pas le traitement par FYREMADEL à moins que cela ne soit conseillé par votre médecin, car cela peut affecter le résultat de votre traitement.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin, à votre pharmacien ou à votre infirmier/ère.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Très Fréquent (pouvant affecter plus de 1 femme sur 10) :
· des réactions cutanées locales (essentiellement une rougeur, accompagnée ou non de gonflement) au point d'injection. La réaction locale disparaît normalement dans les 4 heures suivant l’administration.
Peu fréquent (pouvant affecter jusqu’à 1 femme sur 100) :
· maux de tête ;
· nausées ;
· malaises.
Très rare (pouvant affecter jusqu’à 1 femme sur 10 000) :
· des réactions allergiques ont été observées, dès la première dose.
· éruption cutanée ;
· gonflement du visage ;
· difficulté à respirer (dyspnée) ;
· gonflement du visage, des lèvres, de la langue et/ou de la gorge pouvant provoquer des difficultés à respirer et/ou à avaler (angio-œdème et/ou anaphylaxie) ;
· urticaire.
De plus, ont été rapportés des effets indésirables connus pour survenir pendant un traitement par hyperstimulation ovarienne contrôlée par exemple :
· douleurs abdominales ;
· syndrome d'hyperstimulation ovarienne (SHSO). Le SHSO survient lorsque vos ovaires réagissent de manière excessive aux médicaments contre l'infertilité que vous prenez ;
· grossesse extra-utérine (lorsque l’embryon se développe en dehors de l’utérus) ;
· et fausse-couche (voir la notice patient de la préparation contenant de la FSH avec laquelle vous êtes traitée).
Une aggravation d’une éruption de la peau préexistante (eczéma) a été rapportée chez un sujet après la première dose de FYREMADEL.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, à votre pharmacien ou à votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet: https://signalement.social-sante.gouv.fr.
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER FYREMADEL 0,25 mg/0,5 mL solution injectable en seringue pre-remplie ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur la boîte et sur l’étiquette après « EXP ». La date de péremption fait référence au dernier jour de ce mois.
Ce médicament ne nécessite pas de précautions particulières de conservation.
Examinez la seringue avant utilisation. N’utilisez la seringue que si la solution est limpide, ne contient pas de particules et que si son conditionnement n’a pas été endommagé.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient FYREMADEL 0,25 mg/0,5 mL, solution injectable en seringue pré-remplie ?
· La substance active est l’acétate de ganirélix.
1 seringue pré-remplie de 0,5 mL contient 0,25 mg de ganirélix (sous forme d’acétate).
· Les autres composants sont :
Acide acétique glacial (E260), mannitol (E421), eau pour préparations injectables hydroxyde de sodium et/ou acide acétique glacial (pour ajustement du pH).
Ce médicament se présente sous la forme d’une solution injectable, en seringue pré-remplie. La solution est aqueuse, limpide et incolore. Elle est prête à l’emploi et destinée à une administration sous-cutanée. Le capuchon de l’aiguille contient du caoutchouc naturel sec/latex qui entre en contact avec l’aiguille.
Il est disponible en boîtes contenant 1 ou 5 seringue(s) pré-remplie(s) munie(s) d’une aiguille (27 G).
Titulaire de l’autorisation de mise sur le marché
SUN PHARMACEUTICAL INDUSTRIES EUROPE B.V.
POLARISAVENUE 87
2132 JH HOOFDDORP
PAYS-BAS
Exploitant de l’autorisation de mise sur le marché
7 RUE JEAN-BAPTISTE CLEMENT
94250 GENTILLY
SUN PHARMACEUTICAL INDUSTRIES EUROPE B.V.
POLARISAVENUE 87
2132 JH HOOFDDORP
PAYS-BAS
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen sous les noms suivants : Conformément à la réglementation en vigueur.
[À compléter ultérieurement par le titulaire]
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
< {MM/AAAA}>< {mois AAAA}.>
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).