
ANSM - Mis à jour le : 17/08/2020
UMULINE NPH KWIKPEN 100 UI/mL, suspension injectable
2. COMPOSITION QUALITATIVE ET QUANTITATIVE 
1 mL contient 100 UI d’insuline humaine (produite dans Escherichia coli par la technique de l’ADN recombinant).
Un stylo pré-rempli contient 3 mL correspondant à 300 UI d’insuline isophane.
Pour la liste complète des excipients, voir rubrique 6.1.
Suspension injectable en stylo pré-rempli.
UMULINE NPH est une suspension stérile formée d’un précipité blanc cristallisé, d’insuline humaine isophane dans un tampon phosphate isotonique.
4.1. Indications thérapeutiques 
4.2. Posologie et mode d'administration 
La posologie est déterminée par le médecin, selon les besoins du patient.
Population pédiatrique
Aucune donnée n’est disponible.
Mode d’administration
UMULINE NPH en stylo pré-rempli convient uniquement pour des injections sous-cutanées. Cette spécialité ne doit pas être administrée par voie intraveineuse.
L’administration sous-cutanée doit être effectuée dans les bras, les cuisses, les fesses ou l’abdomen. Il est nécessaire de varier les points d’injection afin de ne pas utiliser le même point d’injection plus d’une fois par mois environ afin de diminuer le risque de développer une lipodystrophie ou une amyloïdose cutanée (voir rubriques 4.4 et 4.8).
Lors de l’injection de toute préparation d’insuline UMULINE, s’assurer que l’aiguille n’a pas pénétré dans un vaisseau sanguin. Après l’injection, ne pas masser le point d’injection. Les patients doivent être éduqués pour utiliser une technique d’injection correcte.
Chaque boîte contient une notice d’information contenant des instructions pour pratiquer l’injection d’insuline.
Hypoglycémie.
Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1, sauf dans le cadre d’un programme de désensibilisation.
Les préparations d’UMULINE ne doivent en aucun cas être administrées par voie intraveineuse, à l’exception d’UMULINE RAPIDE (insuline soluble).
4.4. Mises en garde spéciales et précautions d'emploi 
Les patients recevant de l’insuline humaine peuvent nécessiter un changement de posologie par rapport à leurs insulines d’origine animale. Si une adaptation posologique est nécessaire, elle peut être faite lors de la première administration ou au cours des premières semaines ou des premiers mois.
Quelques patients ayant présenté des réactions hypoglycémiques après transfert d’une insuline d’origine animale à une insuline humaine ont signalé que les symptômes précurseurs d’hypoglycémie étaient moins prononcés ou différents de ceux ressentis lors de leur traitement antérieur par l'insuline animale. Les patients dont la glycémie s’est améliorée de façon importante, par exemple grâce à l’insulinothérapie intensifiée, peuvent voir disparaître certains ou tous les symptômes précurseurs d’hypoglycémie et doivent donc en être informés. La modification ou la diminution des symptômes précurseurs d’hypoglycémie peut également survenir chez les patients présentant un diabète de longue durée, une neuropathie diabétique ou prenant simultanément d'autres médicaments tels que les bêta-bloquants. L'hypoglycémie non corrigée ou les réactions d'hyperglycémie peuvent entraîner une perte de connaissance, un coma ou le décès.
L’utilisation de posologies mal adaptées ou l’arrêt du traitement, en particulier chez les diabétiques insulino-dépendants, peuvent entraîner une hyperglycémie et une acido-cétose diabétique dont le pronostic peut être fatal.
Le traitement par insuline humaine peut provoquer la formation d’anticorps, mais leurs taux sont inférieurs à ceux observés avec l'insuline animale purifiée.
Les besoins en insuline peuvent changer de façon significative en cas de maladies surrénalienne, hypophysaire ou thyroïdienne et d’insuffisance rénale ou hépatique.
Les besoins en insuline peuvent augmenter au cours d’une maladie ou de perturbations affectives.
L’adaptation posologique peut être nécessaire si le patient modifie l’intensité de son activité physique ou modifie son régime alimentaire habituel.
Les patients doivent avoir pour instruction d’effectuer une rotation continue des sites d’injection afin de réduire le risque de développer une lipodystrophie ou une amyloïdose cutanée. Il existe un risque potentiel d’absorption retardée de l’insuline et d’aggravation du contrôle de la glycémie suite à des injections d’insuline au niveau de sites présentant ces réactions. Il a été rapporté qu’un changement soudain du site d’injection vers une zone non affectée entraîne une hypoglycémie. La surveillance de la glycémie est recommandée après changement du site d’injection, et un ajustement de la dose des médicaments antidiabétiques peut être envisagé.
Association d’insuline humaine avec la pioglitazone
Des cas d’insuffisance cardiaque ont été observés lorsque l’insuline était associée à la pioglitazone, en particulier chez des patients ayant des facteurs de risque de développement d’insuffisance cardiaque. Cela devra être pris en compte dans le cas où un traitement associant la pioglitazone et l’insuline humaine est envisagé. Dans ce cas, l’apparition de signes et symptômes d’insuffisance cardiaque, d’une prise de poids et d’œdèmes devra être surveillée chez ces patients. La pioglitazone doit être arrêtée en cas d'aggravation des symptômes cardiaques.
Instructions pour l’utilisation et la manipulation
Afin de prévenir la transmission éventuelle de maladies, chaque stylo doit être utilisé uniquement par un seul patient, même si l’aiguille est changée.
Afin d'améliorer la traçabilité des médicaments biologiques, le nom et le numéro de lot du produit administré doivent être clairement enregistrés.
Excipients
Ce médicament contient moins de 1 mmol (23 mg) de sodium par dose, c.-à-d. qu’il est essentiellement « sans sodium ».
4.5. Interactions avec d'autres médicaments et autres formes d'interactions 
Les besoins en insuline peuvent être augmentés par les substances à effet hyperglycémiant, telles que les glucocorticoïdes, les hormones thyroïdiennes, l’hormone de croissance, le danazol, les bêta-2 mimétiques (tels que ritodrine, salbutamol, terbutaline), les thiazidiques.
Les besoins en insuline peuvent être diminués en présence de substances à effet hypoglycémiant, telles que les hypoglycémiants oraux (ADO), les salicylés (par exemple l’acide acétylsalicylique), certains antidépresseurs (les inhibiteurs de la monoamine oxydase IMAO), certains inhibiteurs de l’enzyme de conversion de l’angiotensine (IEC) (captopril, enalapril), les antagonistes des récepteurs de l’angiotensine II, les agents bêta-bloquants non sélectifs et l'alcool.
Les analogues des somatostatines (octréotide, lanréotide) peuvent réduire ou accroître les besoins en insuline.
4.6. Fertilité, grossesse et allaitement 
Grossesse
Il est essentiel de maintenir un bon équilibre glycémique chez la patiente traitée par l’insuline (diabète insulino-dépendant ou gestationnel) durant la grossesse. Les besoins en insuline chutent habituellement au cours du premier trimestre et augmentent au cours des deuxième et troisième trimestres. Les patientes diabétiques doivent informer leur médecin si elles sont enceintes ou si elles envisagent une grossesse.
Une surveillance attentive de la glycémie ainsi que de l’état de santé général est primordiale pendant la grossesse chez les patientes diabétiques.
Allaitement
Les patientes diabétiques allaitant peuvent nécessiter une adaptation de la dose d’insuline, de leur régime alimentaire ou des deux.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines 
Les patients doivent être informés des précautions à prendre avant de conduire pour éviter une hypoglycémie, en particulier chez ceux chez qui les symptômes précurseurs d’hypoglycémie sont absents ou diminués ou chez ceux qui ont de fréquents épisodes d’hypoglycémie. La capacité à conduire un véhicule doit être réévaluée dans ces circonstances.
L’hypoglycémie est l’effet indésirable le plus fréquent lors du traitement insulinique chez le patient diabétique. L’hypoglycémie sévère peut entraîner la perte de connaissance allant dans des cas extrêmes jusqu'à la mort. L’hypoglycémie pouvant résulter à la fois d’un excès d’insuline et d’autres facteurs tels que l’apport alimentaire et la dépense énergétique, aucune fréquence de survenue des hypoglycémies ne peut être présentée.
L’allergie locale est fréquente (≥ 1/100 à < 1/10). Une rougeur, un œdème et des démangeaisons peuvent survenir au point d’injection. Cette réaction disparaît habituellement en quelques jours voire quelques semaines. Dans certains cas, ces réactions locales peuvent être liées à des facteurs autres que l’insuline, tels que des produits irritants contenus dans le désinfectant cutané ou une mauvaise technique d’injection.
L’allergie systémique, qui est très rare (< 1/10 000) mais potentiellement plus grave, correspond à une allergie généralisée à l’insuline. Elle peut entraîner une éruption généralisée sur tout le corps, une dyspnée, une respiration sifflante, une baisse de la pression artérielle, une accélération du pouls ou des sueurs. Les cas sévères d’allergie généralisée peuvent menacer le pronostic vital. Dans les rares cas d’allergie sévère à UMULINE, un traitement doit être instauré immédiatement. Un changement d’insuline ou une désensibilisation peut être nécessaire.
Une lipodystrophie au site d'injection apparaît peu fréquemment (≥ 1/1 000 à < 1/100).
Affections de la peau et du tissu sous-cutané : fréquence « indéterminée » : Amyloïdose cutanée.
Affections de la peau et du tissu sous-cutané :
Une lipodystrophie et une amyloïdose cutanée peuvent survenir au site d’injection, ce qui peut retarder la résorption locale de l’insuline. Une rotation continue des sites d’injection dans une zone donnée peut aider à diminuer ou à éviter ces réactions (voir rubrique 4.4).
Des cas d’œdèmes ont été rapportés lors du traitement par insuline, en particulier si un mauvais contrôle métabolique précédent est amélioré par une insulinothérapie intensifiée.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : www.signalement-sante.gouv.fr
Il n’existe aucune définition spécifique du surdosage insulinique. En effet, la glycémie résulte d’interactions complexes entre les concentrations d’insuline, la disponibilité du glucose et d’autres facteurs métaboliques. L’hypoglycémie peut résulter d’un excès d’insuline par rapport à l’apport alimentaire et à la dépense énergétique.
L’hypoglycémie peut être associée à une apathie, une confusion, des palpitations, des céphalées, des sueurs et des vomissements.
Les épisodes d’hypoglycémie légère seront compensés par l’administration orale de glucose ou d’autres produits sucrés.
Une hypoglycémie modérément sévère peut être corrigée par l’administration intramusculaire ou sous-cutanée de glucagon, suivie d’une prise orale d’hydrates de carbone lorsque le patient sera suffisamment rétabli. Les patients qui ne répondent pas au glucagon doivent recevoir une solution de sérum glucosé par voie intraveineuse.
En cas de coma hypoglycémique, le glucagon devra être administré par voie intramusculaire ou sous-cutanée. Cependant, s’il n’y a pas de glucagon disponible ou si le patient n’y répond pas, on injectera du sérum glucosé par voie intraveineuse. Dès que le patient aura repris connaissance, un repas lui sera donné.
La prise prolongée d’hydrates de carbone et une surveillance peuvent être nécessaires car une hypoglycémie peut survenir après un rétablissement clinique apparent.
5. PROPRIETES PHARMACOLOGIQUES 
5.1. Propriétés pharmacodynamiques 
UMULINE NPH est une préparation d’insuline d’action intermédiaire.
L’activité principale de l’insuline est la régulation du métabolisme glucidique.
D'autre part, l'insuline possède plusieurs actions anaboliques et anticataboliques dans différents tissus. Dans le muscle, ces effets comprennent une augmentation de la synthèse du glycogène, des acides gras, du glycérol, des protéines et une augmentation de la fixation des acides aminés, ainsi qu’une diminution de la glycogénolyse, de la néoglucogénèse, de la cétogénèse, de la lipolyse, du catabolisme protéique et de l’élimination des acides aminés.
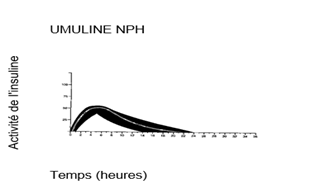
Le profil d’activité type (courbe d’utilisation du glucose) après injection sous-cutanée est représenté sur la courbe ci-dessous par la ligne épaisse. Les variations en durée et/ou intensité d’activité de l’insuline chez les patients sont représentées par la zone sombre. La variabilité individuelle dépend de facteurs tels que la dose, le site d’injection, la température et l’activité physique du patient.
5.2. Propriétés pharmacocinétiques 
5.3. Données de sécurité préclinique 
Glycérol,
Phénol,
Sulfate de protamine,
Phosphate disodique heptahydraté,
Oxyde de zinc,
Eau pour préparations injectables.
Peuvent être utilisés pour ajuster le pH : Acide chlorhydrique et/ou hydroxyde de sodium.
Stylos pré-remplis non utilisés : 3 ans.
Après première utilisation : 28 jours.
6.4. Précautions particulières de conservation 
Stylos pré-remplis non utilisés
A conserver au réfrigérateur (entre 2°C et 8°C). Ne pas congeler. Ne pas exposer à une chaleur excessive ou au soleil.
Après première utilisation
A conserver à une température ne dépassant pas 30°C. Ne pas réfrigérer. Le stylo pré-rempli ne doit pas être conservé avec l’aiguille vissée dessus.
6.5. Nature et contenu de l'emballage extérieur 
3 mL de suspension en cartouche (verre de type I) avec une tête de piston (caoutchouc) à l’extrémité inférieure et une bague ronde (caoutchouc) à l’extrémité supérieure en stylo pré-rempli.
Boîte de 5 ou de 6 ou emballage multiple de 10 (2 x 5).
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation 
Ne pas réutiliser les aiguilles. Eliminer l’aiguille de manière responsable. Les aiguilles et les stylos ne doivent pas être partagés. Le stylo UMULINE NPH KWIKPEN peut être utilisé jusqu’à ce qu’il soit vide, puis doit être convenablement jeté. Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
Instructions pour l’utilisation et la manipulation
Afin de prévenir la transmission éventuelle de maladies, chaque stylo doit être utilisé uniquement par un seul patient, même si l’aiguille est changée.
Suspension injectable en stylo injecteur pré-rempli jetable, contenant une cartouche de 3 mL. UMULINE NPH KWIKPEN délivre jusqu’à 60 unités en une dose et par palier de 1 unité.
a) Préparation d’une dose
Immédiatement avant utilisation, faire rouler 10 fois entre la paume des mains le stylo UMULINE KWIKPEN contenant UMULINE NPH puis retournez-le 10 fois à 180°, afin de remettre l’insuline en suspension, jusqu’à ce qu’elle prenne un aspect uniformément trouble ou laiteux. Si cet aspect n’est pas obtenu, répétez la procédure ci-dessus jusqu’à ce que le contenu soit bien mélangé. Les cartouches contiennent une petite bille de remise en suspension pour faciliter le mélange. Ne pas agiter vigoureusement car la formation d’une mousse pourrait gêner la mesure exacte de la dose.
Examinez les stylos pré-remplis régulièrement et ne pas les utiliser si la suspension présente des floculations ou si des particules blanches restent collées au fond ou sur les parois de la cartouche, lui donnant un aspect givré.
Les cartouches ne sont pas conçues pour la réalisation d’un mélange avec d’autres insulines. Les cartouches vides ne sont pas conçues pour être réutilisées.
Suivre les instructions du stylo UMULINE NPH KWIKPEN pour fixer l’aiguille et pratiquer l’injection d’insuline.
Avec UMULINE NPH KWIKPEN, une aiguille doit toujours être fixée sur celui-ci avant de purger, sélectionner et injecter une dose d’insuline.
UMULINE NPH KWIKPEN doit toujours être purgé avant chaque injection. Ne pas purger le stylo UMULINE NPH KWIKPEN peut entraîner une dose inexacte.
b) Injection d’une dose
Injectez la dose correcte d’insuline en suivant les instructions du médecin ou de l’infirmier/ère spécialiste du diabète.
Il est nécessaire de varier les points d’injection pour que le même site ne soit pas utilisé plus d’une fois par mois environ.
Chaque boîte contient une notice d’information contenant des instructions pour pratiquer l’injection d’insuline.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE 
24, BOULEVARD VITAL BOUHOT
CS 50004
92521 NEUILLY-SUR-SEINE CEDEX
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE 
· 34009 348 788 2 4 : 3 mL de suspension injectable en stylo pré-rempli ; boîte de 5.
· 34009 496 506 5 1 : 3 mL de suspension injectable en stylo pré-rempli ; 2 boîtes de 5.
· 34009 301 477 8 8 : 3 mL de suspension injectable en stylo pré-rempli ; boîte de 6.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION 
[À compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE 
[À compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES 
Liste II
|
| Plan du site | Accessibilité | Contact | Téléchargement | Declaration de confidentialité | Service-Public.fr | Legifrance | Gouvernement.fr |